2026年度の申請期間は、2026年6月30日までとなっております。申請の期限を過ぎて応募された場合は、受理できませんので、ご留意ください。
研究者主導臨床研究公募プログラム
研究者主導臨床研究への支援について
当社は、「臨床研究法」または「人を対象とする生命科学・医学系研究に関する倫理指針」に則り実施される、当社の指定した領域、薬剤、テーマに関する研究者主導臨床研究に対して公募を行い、研究費の支援を実施いたします。
申請いただいた臨床研究提案につきましては、申請要項に基づき当社内において公正・中立な審査により支援の可否を判断し、支援の対象と決定された臨床研究に対して契約に基づく研究費の支援を実施いたします。学術研究の振興や研究助成を目的として行われる奨学寄附金ではありません。
対象とする臨床研究
当社が指定する以下の領域、薬剤又は疾患、テーマを対象とします。薬剤の使用にあたっては医薬品医療機器等法による承認の範囲内の効能・効果、用法・用量に限ります。
この表はスクロールしてご覧いただけます
| 領域 | 薬剤又は疾患 | テーマ |
|---|---|---|
| 血液・がん | ロミプロスチム(再生不良性貧血) | 再生不良性貧血に対するロミプロスチムの有用性について |
| 腎 | テナパノル(透析中の慢性腎臓病患者における高リン血症) | 透析中の慢性腎臓病患者における高リン血症に対するテナパノルの有用性について |
| ダプロデュスタット(腎性貧血) |
保存期慢性腎臓病患者および透析患者における腎性貧血に対するHIF-PH阻害薬の有用性について
|
|
| 先天性代謝異常疾患 | 異染性白質ジストロフィー(MLD) |
|
申請~終了までのプロセス

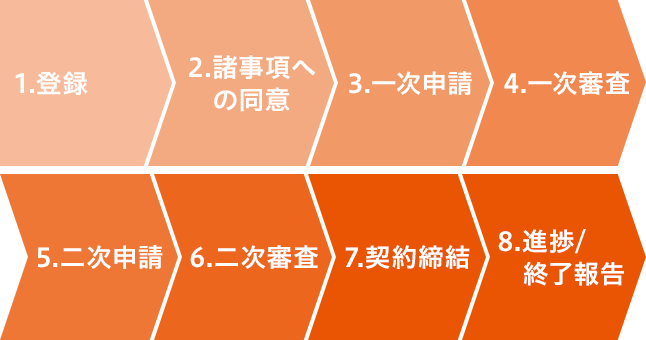
- 1. 登録
- 臨床研究提案を申請いただくために、まずアカウントの登録を実施いただきます。
- 2. 諸事項への同意
- 臨床研究提案を申請いただく前に、いくつかの確認事項に対して同意いただきます。
- 3. 一次申請
- 一次申請では研究内容を入力いただくほか、「研究費用の見積書(概算)(日本語)」を提出いただきます。
- 4. 一次審査
- 主に申請された臨床研究の内容、費用について審査を行います。
- 5. 二次申請
- 一次審査を通過した臨床研究提案について、「研究概要(英語)」、「研究責任者の履歴書(英語)」、「研究計画書(日本語)」、「研究費用の見積書(詳細)(日本語)」を提出いただきます。
- 6. 二次審査
- 主に申請された臨床研究の詳細、実施体制、要件について審査を行います。
- 7. 契約締結
- 臨床研究の契約を締結します。
- 8. 進捗/終了報告
- 締結した契約に従って、進捗/終了の報告をしていただきます。
応募、お問い合わせの際には、アカウントの取得が必要になりますことをご了承ください。
