本記事は協和キリンアニュアルレポート2022より再構成したものです。
社会との共有価値確かな品質の医薬品の安定供給
確かな品質の医薬品を安定的に供給すること、これは製薬企業にとって何よりも大切なことだと考えています。
協和キリンは「製品の品質保証と安定供給」をマテリアリティ(重要経営課題)に掲げ、さまざまな取り組みを進めています。
安定供給を目指した高崎工場への設備投資
協和キリンは群馬県高崎市と山口県宇部市の2か所に基幹生産拠点を有しています。高崎地区は主にバイオ医薬品を扱う拠点であり、生産技術開発と承認申請業務を行う「バイオ生産技術研究所」と治験薬および上市品の原薬製造と製剤化を行う「高崎工場」があります。隣接するメリットを活かし、お互いに協力しながら、世界屈指のバイオ医薬品研究・製造拠点として全員が一丸となって業務に取り組んでいます。
「Q-TOWER」が竣工
2022年には高崎工場に建設していた「Q-TOWER」が竣工しました。Q-TOWERはバイオ医薬品の製品・原料の分析など品質管理および品質保証に関連する業務を行うために新たに建設した、日米欧のGMP/Good Manufacturing Practiceに準拠した施設です。この施設は、自動コロニーカウンター、微生物迅速試験装置、ロボットテクノロジーなどの国内最先端のバイオ医薬品分析設備や、リキッドハンドリングシステム、サンプル自動ピッキングシステムなどの自動化・省力化設備を備え、また、無菌試験用アイソレータを導入し、最新のレギュレーションに対応した試験施設設計を実現しています。加えて、空間に連続性を持たせた執務空間のデザインにより、誰もが健康的に、創造的に、相互理解のもとで働ける環境を整備し、本施設で業務する従業員にとって最適なワークプレイスとなっています。

新原薬製造棟および新倉庫棟の建設を計画中
2022年には、高崎工場に新バイオ医薬原薬製造棟および新倉庫棟を建設することを決定しました。
新原薬棟「HB7」は、独自の抗体技術やたんぱく工学を活用したバイオ医薬品の原薬製造に対応し、GMPに則り臨床試験で使用するための原薬を製造するGMP製造設備と、研究所で構築した製造方法をスケールアップ検証するためのパイロット設備の両方を有します。両設備はシングルユース設計となっており、原薬製造の初期プロセス開発から治験原薬の製造までを同一設備構成で実施できることから、少量多品目の初期開発品をよりフレキシブルに、かつ迅速に製造することが可能になります。パイロット設備では、安定供給に向けた技術革新の一環として、新しいバイオ医薬品製造技術である連続生産方式の検証も計画しています。


新倉庫棟は、バイオ医薬品(製品および開発品)の供給拡大に対応するために建設します。医薬品の原材料、原薬や製剤の保管については、厳重な管理対策を講じることが各国の規制当局から求められています。そのため、新倉庫棟は、各規制当局の基準を順守し、常温、冷蔵、冷凍のいずれの温度でも安定してバイオ医薬品の原材料、原薬や製剤を保存することが可能です。また、地震や水害等の大規模な災害が発生した際にも継続的な製品供給や早期の製造再開ができるよう免震構造を有し、重要な設備については浸水による被害から保護できる設計を想定しています。さらに、屋上への太陽光発電設備の設置および省エネ空調機器の積極採用などにより、環境への対応にも考慮した施設になっています。
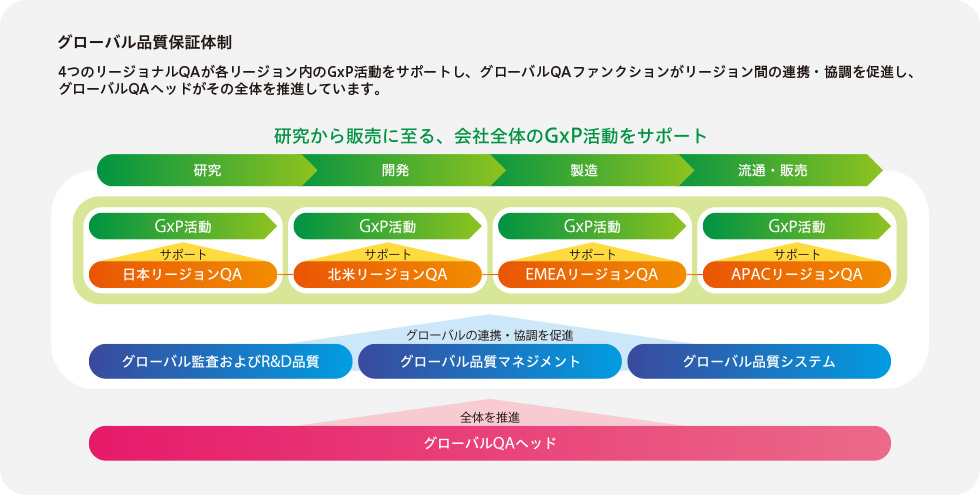
世界水準の品質保証(QA/Quality Assurance)体制の構築
医薬品は人命に直結する製品であり、製薬企業にとって「品質」は従業員一人ひとりの責任です。確かな品質とコンプライアンスなしには、患者さんや医療従事者、各国の規制当局はもちろん、社会全体からの信頼を得ることはできません。協和キリンのQA部門は、製造・流通をはじめとするさまざまな工程が関連法規に準拠して適切に行われていることを確認し、患者さんにお届けする医薬品の品質に問題がないことを保証する役割を担っています。
エンタープライズ/電子品質マネジメントシステム「eQMS」
グローバル化が本格化し始めた2019年以降、私たちは「協和キリングループ品質基本方針」および「2025年に向けたグローバル品質ロードマップ」を策定し、着々とグローバルQA体制の強化を進めてきましたが、2022年には、エンタープライズ/電子品質マネジメントシステム「eQMS」の導入を完了しました。逸脱管理、是正・予防措置(CAPA)、教育、文書管理、監査、サプライヤー管理、変更管理など多岐にわたる品質保証業務を完全な電子プロセスでカバーするこのシステムの導入により、グローバルで一貫した水準をもって各国関連法規の要求を満たすプラットフォームが整ったことになります。また、自信を持って「世界水準」と自負できる、リスクベースアプローチによる予防的品質マネジメントシステムの構築を目指し、グローバルで統合されたKPIを設定し、運用状況をリアルタイムでモニタリングしながら、収集した膨大なデータを集約・解析し、プロセスの継続的改善やクオリティ・カルチャーの醸成などに引き続き取り組みます。
サプライチェーンマネジメント(SCM)やその他の取り組み
Crysvitaを中心とするグローバル戦略品の販売国はますます拡大し、2020年には48%だった海外売上収益比率は、2023年には64%に達する見込みです。これに伴い、委託先も含めた製造・物流に関係するサプライチェーンはますます複雑化しており、協和キリンはそのマネジメントに力を入れて取り組んでいます。
協和キリンのSCM部門は、私たちの医薬品を必要とする患者さんに必要なときに必要なだけ確実に届けるため、この複雑な状況を的確に把握・コントロールする役割を担っています。高い精度で需給バランスをコントロールするため、SCM部門がコーディネート役となり、内部では特に品質部門・生産部門・販売部門と、また、外部では製造委託会社や物流会社などとの強力なパートナーシップを構築しています。同時にS&OP*の取り組みを進化させ、マネジメントによる迅速な意思決定と在庫水準の適正化に貢献しています。
2020年に始まった新型コロナウイルス感染症に伴う混乱に続き、2022年にはロシア・ウクライナ紛争に伴う輸送リスクが発生しましたが、SCM部門を中心とした連携・対応により、協和キリンは安定的に供給を続けています。今後もこれを継続すべく、サプライチェーンに関するKPIモニタリングによる早期の異常検知と継続的な改善に加え、安定供給BCP(Business Continuity Plan/事業継続計画)の構築・アップデート、原薬保管拠点の複数化など、安定供給に向けたさまざまな施策を計画しています。また、昨今ますます大きな問題となっている偽造医薬品問題への対策もさらに拡大し、患者さんが安心して治療を受けられる環境づくりに貢献していきます。
*Sales and Operations Planningの略。販売部門と生産・オペレーション部門の間で、計画・実績を数量と金額の両面で確認し、会社にとって最適な計画に合意する仕組みのことで、意思決定の精度とスピードを高め、財務目標の達成を促進します。